صدور عجولانه مجوز مصرف اضطراری واکسنهای ایرانی و بدگمانی مردم
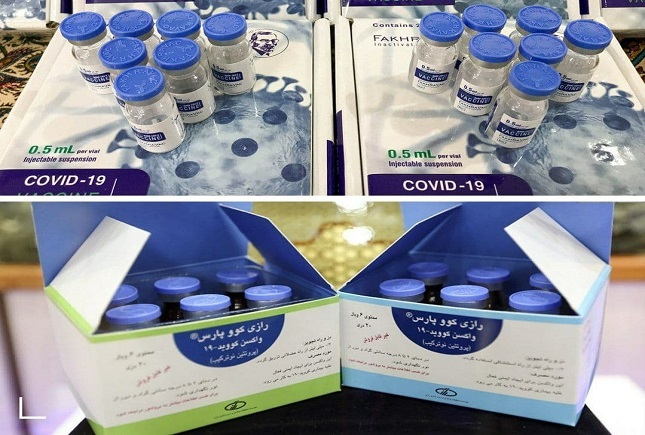
به گزارش جامعه ۲۴، روز یکشنبه سازمان غذا و دارو مجوز مصرف اضطراری دو واکسن کووپارس از مؤسسه سرم سازی رازی و واکسن فخرا از وزارت دفاع را صادر کرد. صدور مجوز این واکسن در حالی صورت میگیرد که تا دو روز قبل از آن مقاومت موسسه رازی در ارائه مستندات واکسن خود به سازمان غذا و دارو و همچنین عدم تمایل وزارت بهداشت برای خرید واکسن فخرا در صدر اخبار مربوط به حوزه سلامت بود.
از سوی دیگر هر دوی این واکسنها در مرحله سوم کارآزمایی بالینی خود قرار داشته و گفته میشد با کمبود داوطلب برای این مرحله با توجه به افزایش سطح واکسیناسیون در جامعه مواجه شدهاند.
صدور سریع مجوز مصرف اضطراری واکسنها و عدم چاپ مقالات این واکسنها نگرانیها و انتقاداتی را به وجود آورده است.
تعجیل در صدور مجوز مصرف اضطراری واکسن
علیرضا ناجی، رئیس مرکز تحقیقات ویروس شناسی دانشگاه علوم پزشکی شهید بهشتی در صفحه اینستاگرام خود با اشاره به اینکه واکسنهای ایرانی بدون طی کردن کامل مرحله سوم کارآزمایی بالینی به سرعت مجوز میگیرند در حالی که دسترسی خوبی به واکسنهای خارجی مجوزدار داریم، از صدور مجوز مصرف اضطراری این دو واکسن انتقاد کرد و نوشت: در خبرها آمده مجوز با قبول مسئولیت شرکت سازنده در عوارض صادر شده است. اصلا این چه معنایی دارد؟ این عجله برای چیست؟
مجوز مصرف اضطراری واکسن بدون اتمام کارآزمایی بالینی
ناجی هم با بیان اینکه در صدور مجوز مصرف واکسنها در حالی که هنوز در مراحل کارآزمایی بالینی هستند عجله شده است، اظهار کرد: ما هنوز کارآزمایی بالینی واکسنها را به اتمام نرساندیم. بسیار دیر به کارآزمایی آنها پرداختیم و همزمان چندین واکسن را نیز در دست تولید داریم؛ لذا صدور مجوز مصرف اضطراری در این شرایط درست نیست.
بیشتر بخوانید: شناسایی واکسن نزدهها از دو هفتهی دیگر
وی افزود: ما در کشورمان با این قیاس اقتصادی و با صرف این همه هزینه اقدام به تولید و توسعه این تعداد واکسن کووید میکنیم که حتی در به پایان رساندن مراحل کارآزمایی بالینیاش ناتوانیم و بعد میآییم و انتقاد میکنیم که دولت به ما قول خرید آن را داده و برای آن هزینه کردهایم پس حال که چنین است باید به ما مجوز مصرف بدهند.
ناجی ادامه داد: اگر به جای تمرکز به تعدد واکسنها با پلتفرمهای مشابه، بر روی یک یا دو واکسن تمرکز میکردیم هم زودتر به نتیجه میرسیدیم و هم اینکه واکسن هم زودتر به مردم میرسید. از سوی دیگر میتوانستیم همانند کاری که پاستور انجام داد با مشارکت شرکتهای بزرگ واکسن سازی به توسعه و تولید واکسنها بپردازیم تا هم از تهدید کرونا فرصت خلق کنیم و هم اینکه تکنولوژی را وارد کشور میکردیم.
لزوم بررسی دقیق واکسنهای ایرانی
وی یادآور شد: اگرچه نمیتوان به عقب بازگشت، اما انتظار میرود که با دقت زیاد به بررسی واکسنهای خود بپردازیم. در این شرایط صدور مجوزهای سریع مصرف اضطراری بدون طی کردن کامل مراحل کارآزمایی بالینی امری اشتباه است و تبعات بدی در اذهان عمومی خواهد داشت.
وی بیان کرد: ما از اول میدانستیم نمیتوانیم تعداد بسیار زیادی واکسن را کارآزمایی بالینی کنیم، چرا که با توجه به شرایط کووید، نیاز بود تعداد زیادی واکسن را از خارج وارد کنیم تا دسترسی مردم به واکسن را افزایش دهیم. وقتی سطح دسترسی مردم به واکسن افزایش پیدا کرد، مشخص بود که در کارآزمایی بالینی واکسنها به مشکل برمیخوریم و مراحل کارآزمایی بالینی هم به خوبی طی نخواهد شد.
بدگمانی در صدور عجولانه مجوز مصرف اضطراری واکسنهای ایرانی
ناجی با بیان اینکه صدور سریع مجوز مصرف اضطراری واکسن های ایرانی کرونا بدون طی کردن مراحل کارآزمایی بالینی ممکن است موجب بدگمانی مردم شود، گفت: اگرچه موسسهای مانند رازی سابق درخشانی در ساخت واکسن دارد و مطمئنا واکسن خوبی را نیز تولید کرده است با این حال این تعجیل در صدور مجوز ممکن است شبهه به وجود آورده و مردم را نسبت به آن بدگمان کند.
































